10
2023
-
11
DEB-TACE联合雷替曲塞治疗不可切除或复发性肝细胞癌的初步疗效
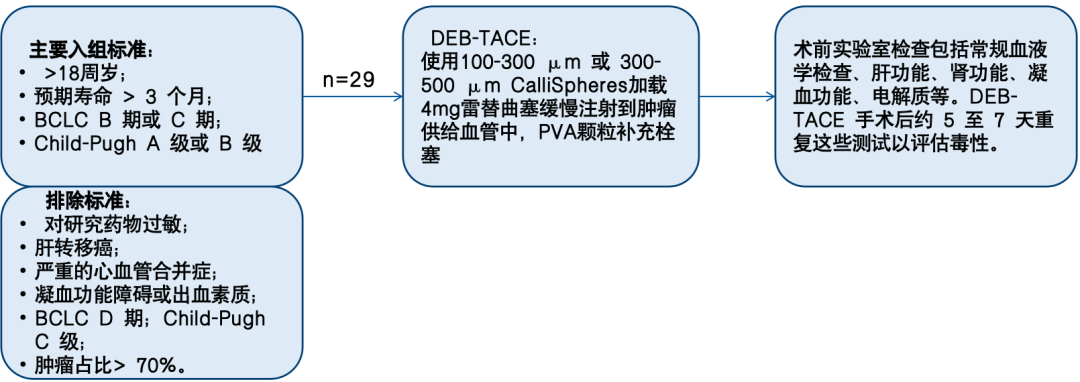
研究类型:一项回顾性研究,2018年6月至2020年3月期间纳入了29例不可切除或复发性HCC患者。旨在探讨装载雷替曲塞的 DEB-TACE 对不可切除或复发性 HCC 患者的初步疗效。
01研究设计
研究类型:一项回顾性研究,2018年6月至2020年3月期间纳入了29例不可切除或复发性HCC患者。旨在探讨装载雷替曲塞的 DEB-TACE 对不可切除或复发性 HCC 患者的初步疗效。
研究设计:
02患者基线
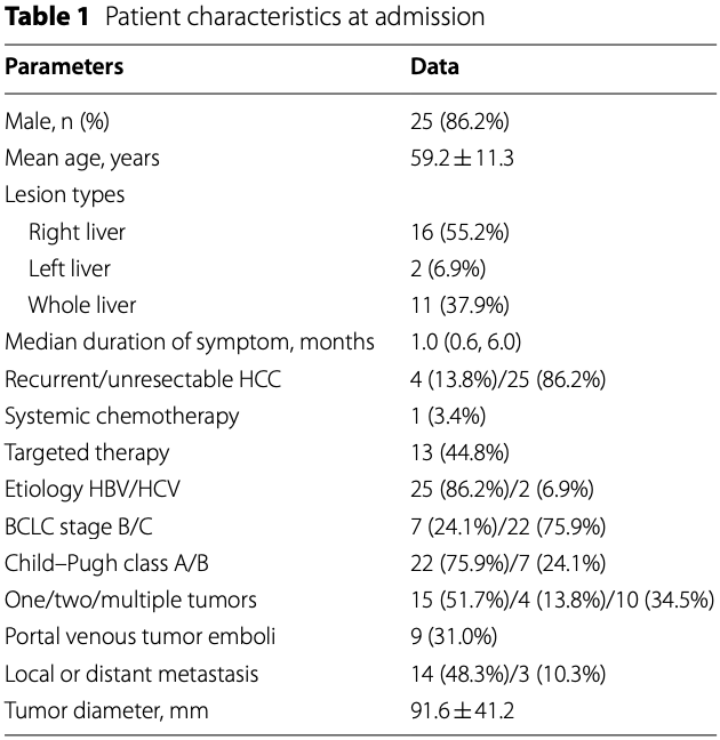
4 名患者(13.8%)患有复发性 HCC,25 名患者(86.2%)患有无法切除的 HCC。15 例(51.7%)患者发现单个肿瘤,4 例(13.8%)患者有两个肿瘤,其余 10 例(34.5%)患者至少有 3 个肿瘤。
03结果
肿瘤反应(ORR、DCR)
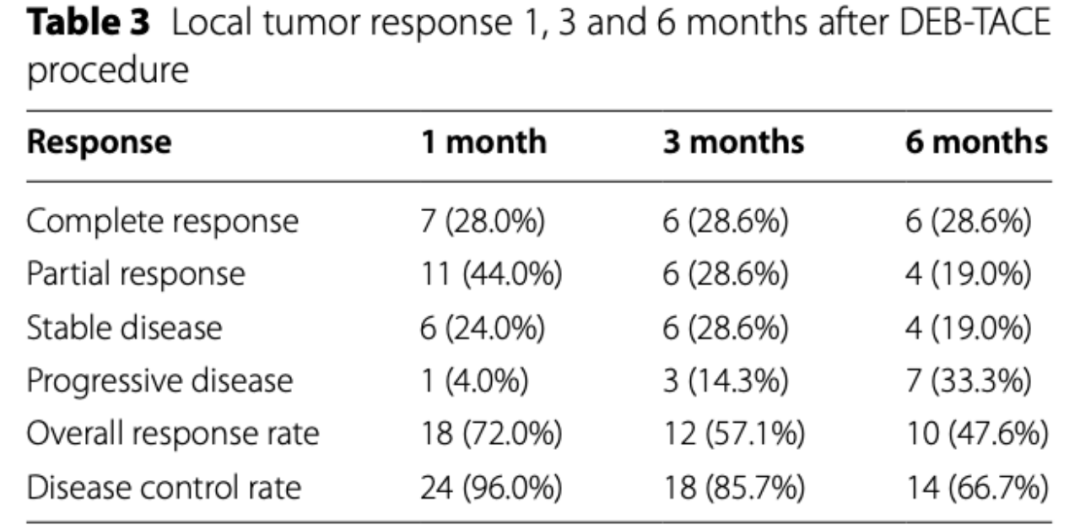
DEB-TACE 后肿瘤增强显着减少。1、3、6个月的ORR分别为72.0%、57.1%、47.6%。1、3、6个月DCR分别为96.0%、85.7%、66.7%。
PFS、OS
平均随访时间为 23.2 ± 18.4 个月。中位无进展生存期为 25.7 个月,6、24 和 36 个月无进展生存率 (PFS) 分别为 72.3%、51.9% 和 37.5%。中位总生存期为33.9个月,6个月、24个月和36个月总生存率分别为88.4%、66.3%和46.3%。
安全性

17 名患者(58.6%)观察到轻微并发症,没有与治疗相关的死亡或严重不良事件。最常见的治疗相关非血液并发症是腹痛 (41.4%) 和 ALT/AST 升高 (27.6%)。所有报告的毒性均为 1 级和 2 级。
04结论
- DEB-TACE联合雷替曲塞对于不可切除的 HCC 患者是安全且可耐受的。没有出现与治疗相关的死亡或严重不良事件。所有报告的毒性均为 1 级和 2 级。
- 这是一项样本量有限且在单一中心进行的回顾性研究,因此存在一些局限性。
版权声明丨
本文旨在分享医疗健康领域最新研究进展,并非治疗方案推荐,仅供医疗专业人士阅读。如需获得专业诊疗指导,请前往正规医院就诊。
本文版权归 微球时代 所有,欢迎转发分享至朋友圈。其他任何个人、媒体或机构如需转载或引用本文章相关内容,须获得授权,且注明文章来源。
推荐新闻
2023-12-26
2023-12-26
2023-12-26
2023-12-26
2023-09-07


